ما هي الأحماض الأمينية؟
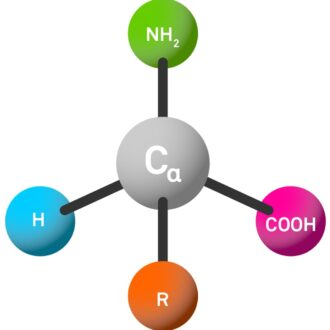
تسمى الأحماض الأمينية الأكثر شيوعًا في الطبيعة الأحماض الأمينية α. تحتوي هذه الجزيئات على أربع بدائل مختلفة متصلة بذرة الكربون المركزية (تسمى ذرة α-C):
الأمينية (NH₂ ، رمز ثلاثة أحرف مختصرة باسم "H-").
مجموعة حمض الكربوكسيل (COOH ، اختصار كـ "-oh" في الكود المكون من ثلاثة أحرف).
سلاسل جانبية(R ، والتي هي متغيرة للغاية وتحدد خصائص الأحماض الأمينية وكذلك الببتيد النهائي).
ذرة الهيدروجين (ح).
يمنحه اتصال ذرات α-C بهذه المجموعات الأربع المختلفة خصائص كيميائية فريدة ، والتي تلعب دورًا رئيسيًا في تحديد سلوك وخصائص الأحماض الأمينية والببتيدات.
النشاط البيولوجي للأحماض الأمينية
يمكن للأحماض الأمينية أن تظهر أنشطة بيولوجية مثل:
تلعب التربتوفان (TRP) وحمض الغلوتاميك (GLU) دورًا رئيسيًا في عمليات التمثيل الغذائي.
تحدد مجموعة R (أو السلسلة الجانبية) الخصائص الفريدة للأحماض الأمينية. يمكن لهذه المجموعات:
بعبارات بسيطة:ذرة الهيدروجين مثل الجليكاين (جلي).
يتم تضمين الأحماض الأخرى: مثل حمض الأسبارتيك (ASP) وحمض الجلوتاميك (GLU).
حمل المجموعات الأساسية:أرجينين (arg) ، ليسين (Lys) أو الهستيدين (له).
يحتوي على مجموعات قطبية: مثل سيرين (سير) أو ثريونين (THR).
الهيدروكربونات غير القطبية:ألانين (ALA) ، فينيل ألانين (PHE) أو Valine (VAL).
محتوى الكبريت:كما رأينا في السيستين (Cys) والميثيونين (Met).
دور الأحماض الأمينو والأحماض الأمينية D
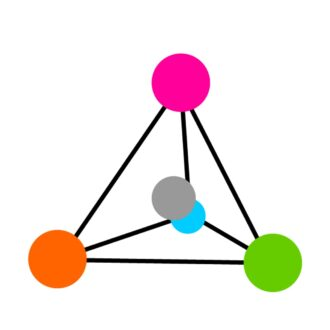
يتم ترتيب البدائل الأربعة لذرة α-C في زوايا رباعي السطوح ، مع ذرة α-C في الوسط (انظر الشكل 3). يسمح هذا الترتيب لشكلين من جزيئات الأحماض الأمينية في شكل مرآة ، على غرار الأيدي اليسرى واليمنى. تُعرف أشكال المرآة هذه باسم "أجهزة الاستريو" أو "enantiomers".
الأهمية البيولوجية للأماكن
على الرغم من أن enantiomers لها خصائص كيميائية وفيزيائية متطابقة تقريبًا ، إلا أن آثارها البيولوجية يمكن أن تختلف اختلافًا كبيرًا. الشكل الجزيئي أمر بالغ الأهمية لتفاعله مع الأهداف البيولوجية. قد يرتبط أحد الأطراف بشكل فعال بالهدف ، أو قد لا يكون له ، أو في بعض الحالات تأثير سلبي. في المحلول ، يدور Enantiomer مستوى الضوء المستقطب في الاتجاه المعاكس.
وقت النشر: 2025-09-05
